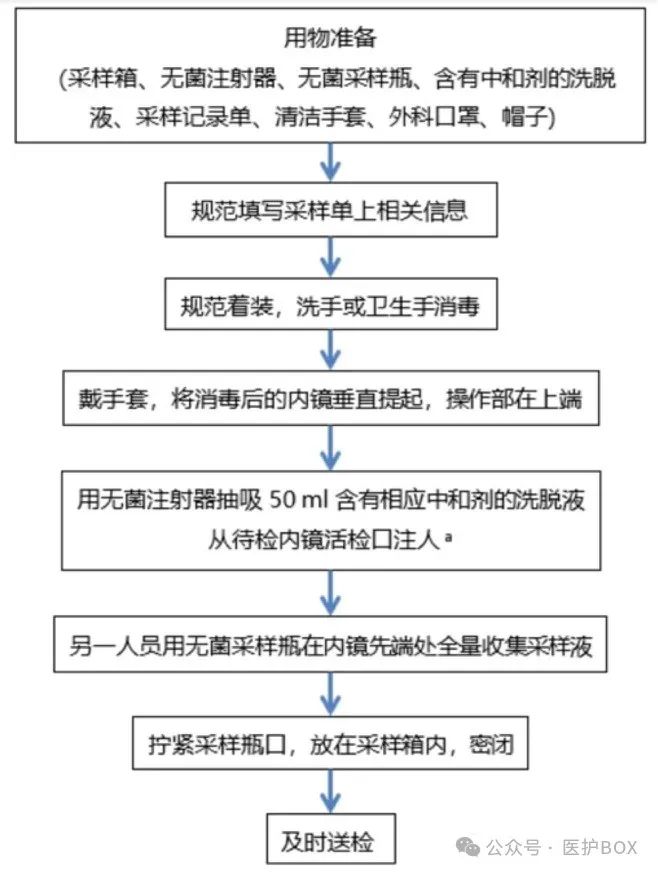
消化内镜再处理质量控制具体有哪些内容?如何进行?发表时间:2024-10-30 08:49 Q 消化内镜再处理质量控制包含哪些内容? 1、常见消化内镜的分类: 1)根据内镜属性分类,常用的有胃镜、十二指肠镜、结肠镜、小肠镜、超声内镜、胶囊内镜等等; 2)按检查部位和功能分为上消化道内镜、下消化道内镜、内镜逆行胰胆管造影(ERCP)及内镜超声; 3)按临床应用分为诊断性消化内镜和治疗性消化内镜。 2、消化内镜再处理质量控制: 主要包括规范内镜操作流程、环境监测、内镜再处理各步骤监控、人力资源管理、人员培训、洗消设备配置、管理制度和可追溯信息化管理等内容。 消化内镜再处理质量控制如何进行? 质量控制是保证消化内镜再处理效果的前提保障,确保再处理程序的安全性、有效性和一致性。 消化内镜再处理的质量控制主要包括以下方面。 (1)遵守规范操作流程:应制订明确的再处理操作规程,并确保所有医护人员都受过规范的培训,熟悉再处理步骤和标准操作程序。 (2)再处理室环境监测:确保再处理室的清洁与消毒,定期进行内镜消毒室的微生物监测,以评估环境清洁和消毒的效果。监测样本应包括表面、空气和水质等,并根据相关规范进行微生物培养和分析。 (3)清洗质量监测:内镜清洗质量的监控是确保内镜再处理程序有效性的关键环节,通过目测检查、蛋白残留测定、ATP生物荧光测定等方法,确保内镜表面清洁,无污垢、蛋白、微生物等残留物质;同时,应定期进行内镜的生物学监测,以评估消毒的效果。 (4)内镜消毒/灭菌质量监测:选择适合的清洗剂和消毒(灭菌)剂,根据制造商的说明正确使用,对使用中的消毒剂和灭菌剂进行定期的浓度监测,并根据每种产品的最低消毒浓度要求及时更换,确保消毒剂和灭菌剂的浓度符合要求,以保证再处理程序的安全性和有效性,并定期进行染菌量监测。 (5)人力资源和设备配置:应当尽可能加强内镜室人员和设备配置,并持续对内镜医护人员和再处理人员进行培训和教育,以保证他们在再处理过程中采取正确的操作和控制措施。 (6)管理制度的制订:建立质量监控机制,同时制订相关文件,通过定期内部或外部审核来评估再处理的质量。 (7)可追溯信息化管理:建立完整的内镜追溯体系,记录内镜的使用情况、清洗和消毒过程等信息。确保对每次再处理过程进行准确的文档记录,这有助于追踪和调查任何潜在的再处理相关问题,并确保合规性和责任追溯。 此外,内镜再处理的设施设备还需严格参照《内镜清洗工作站》(YY/T 0992—2023)的要求执行。 通过以上一系列控制措施,可以最大限度地确保消化内镜再处理的质量,并提供安全和可靠的再处理程序。 内镜清洗消毒质量监测标准操作规程 1、适用范围: 1)评价内镜清洗消毒的效果。 2.)当怀疑医院感染与内镜诊疗操作相关时。 2、采样时间:在洁净系统自净后与从事医疗活动前采样。 3、采集方法:
4、检测方法:将洗脱液充分混匀,取洗脱液1.0ml接种平皿,将冷却至40℃~45 ℃的熔化营养琼脂培养基每皿倾注15~20ml,36±1 ℃恒温箱培养48小时,计数菌落数(CFU/件)。将剩余洗脱液在无菌条件下采用滤膜(0.45μm)过滤浓缩,将滤膜接种于凝固的营养琼脂平板上(注意不要产生气泡),置于36±1 ℃温箱培养48小时,计数菌落数。 5、计算方法及结果判断: 1. 当滤膜法不可计数时:菌落总数(CFU/件)=m(CFU/平板)× 50。 式中:m为两平行平板的平均菌落数。 2. 当滤膜法可计数时:菌落总数(CFU/件)=m(CFU/平板)+ mf(CFU/滤膜)。 式中:m为两平行平板的平均菌落数;mf为滤膜上菌落数 3. 消毒合格标准:≤20CFU/件。但若检出肠杆菌、肠球菌、铜绿假单胞菌和其他非发酵革兰阴性杆菌、葡萄球菌属,应考虑消毒不合格。 6、其他管理要求: 1. 消毒内镜应每季度进行生物学监测,监测采用轮换抽检的方式,每次按25%的比例抽检。内镜数量少于等于5条的,应每次全部监测;多于5条的,每次监测数量应不低于5条。 2. 当怀疑医院感染与内镜诊疗操作相关时,应进行致病性微生物检测。 3. 监测方法应遵循GB15982的规定,消毒合格标准:菌落总数≤20CFU/件。 来源及引用: [1]中华医学会消化内镜学分会清洗消毒学组.中国消化内镜再处理专家共识(2024,重庆)[J].中华消化内镜杂志, 2024, 41(9): 673-684. Cleaning and Disinfection Group, Digestive Endoscopology Branch of Chinese Medical Association.Chinese expert consensus on gastrointestinal endoscope reprocessing (2024, Chongqing)[J].Chin J Dig Endosc, 2024, 41(9): 673-684. DOI: 10.3760/cma.j.cn321463-20240827-00389. [2] 中华人民共和国卫生行业标准.WS 507-2016软式内镜清洗消毒技术规范[ EB/OL].(2017-01-17)[ 2019-01-07]. http:/www.nhfpc.gov.cn/ewebeditor/uploadfile/2017/0020170105090816920.Pdf. [3] 中华人民共和国卫生部,GB 15982-2012医院消毒卫生标准[S]//国家卫生和计划生育委员会医院管理研究所医院感染质量管理与控制中心.医院感染管理文件汇编(1986-2015).北京:人民卫生出版社,2015:125-137. [4] Beilenhoff U,Neumann CS,Rey JF,et al. ESGE-ESGENA guideline for quality assurance in reprocessing:microbiological surveillance testing in endoscopy [J]. Endoscopy,2007,39(2):175-181. 文章转载自医护BOX,如有侵权,联系我们,立即删除。 内容来源:内镜微创达人 —————————————————— 为人类感控事业而奋斗——明誉医疗 |